
1.4.1.3 Rappels sur le Carbone asymétrique:
- Il est porteur de 4 radicaux différents (exemple : C2 du glycéraldéhyde)
- Isomères optiques ou énantiomères
- Isomère dextrogyre (+)
- Isomère lévogyre (-)
- Mélange équimoléculaire des 2 isomères : Racémique (DL) inactif sur la lumière polarisée.
</li>
Une molécule chirale est une molécule optiquement active :
Elle renferme au moins 1 C asymétrique
Elle n'a pas de plan de symétrie.
</li>
Configuration stéréochimique et pouvoir rotatoire d'un ose
En dehors du glycéraldéhyde, il n'y a aucune relation entre configuration stéréochimique de l'ose et son pouvoir rotatoire.
1.4.2 Filiation chimique des oses selon Fischer
- Formation à partir du D-Glycéraldéhyde (par addition de C successifs)
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
- Un Triose
 Deux Tétroses Deux Tétroses
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td>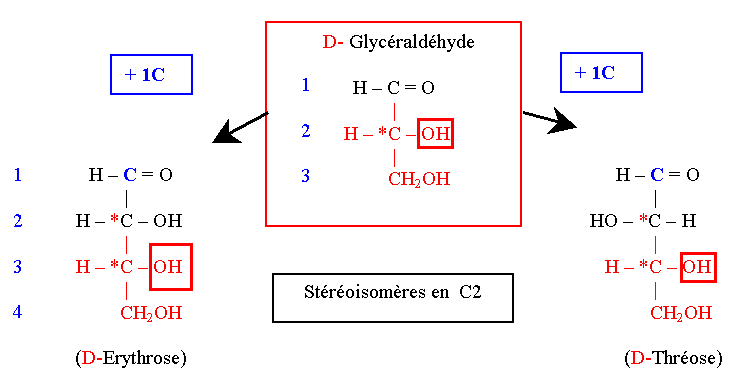 </td> </td>
</tr></table>
1.4.3 Série D et L des oses
- Oses de la série D
- Ils
sont rattachés au D-Glycéraldéhyde : la configuration spatiale de
l'hydroxyle porté par le C subterminal de l'ose (ou Carbone n-1) est
identique à celle du D-Glycéraldéhyde.
- La plus grande majorité des oses naturels sont de la série D.
</li>
Oses de la série L:
Ils dérivent par voie chimique du L-Glycéraldéhyde.
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr>
<tr align="center"><td>Filiation des oses selon Fischer (série D)</td>
</tr></table>
Par addition successive d'un carbone, on obtient à chaque étape la formation de 2 isomères (1 triose  2 tétroses 2 tétroses  4 pentoses 4 pentoses  8 hexoses).1.4.4 Principaux oses naturels selon Fischer: 8 hexoses).1.4.4 Principaux oses naturels selon Fischer:
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
Epimères:
- L'épimérisation se fait par voie chimique ou enzymatique (épimérase).
- Le
Galactose est épimère en 4 du Glucose. L'absence d'épimérase empêche la
transformation du Galactose en Glucose et entraîne une des formes de la
galactosémie congénitale du nouveau-né.
- Le Mannose est épimère en 2 du Glucose (c'est un épimère chimique = épimère vrai).
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td>
1.4.5 Objections à la structure linéaire des oses
- En solution dans l'eau, les oses existent sous forme cyclique
- Nous citerons deux objections à la structure linéaire :
- Formation d'Acétal
- Un aldose ou une cétone vrais fixe deux molécules d'alcool
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
- Un aldose ou un cétose ne fixent qu'une seule molécule d'alcool
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
</li>
- Mutarotation (anomères)
La
valeur du pouvoir rotatoire d'un ose (mesurée au polarimètre) n'est pas
fixée immédiatement ; elle le devient au bout d'un certain temps. Ce
phénomène est lié à l'existence de 2 formes isomériques, l'anomère  ou ß à l'origine de la mutarotation. Ces 2 anomères différent par la position dans l'espace du OH hémiacétalique. ou ß à l'origine de la mutarotation. Ces 2 anomères différent par la position dans l'espace du OH hémiacétalique.
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
- Ces objections permettent de montrer qu'en solution les oses existent non pas sous forme linéaire mais sous forme cyclique.
</li>
1.4.6 Structure cyclique des oses : structure de Haworth
Le cycle est formé par une liaison dans la molécule d'ose entre la
fonction carbonylique (aldéhyde ou cétone) et un OH alcoolique =
liaison hémiacétalique.<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
<table width="84.6153846154%" align="center" border="0" cellpadding="0"><tr align="center"><td><table width="100%" align="center" border="0" cellpadding="5">
<tr align="left" valign="top"><td width="100.0%">La structure est convexe vers l'observateur.
Par cette convexité les C1 et C6 sont proches dans l'espace.
La rotation des valences autour du C5 permet de mettre sur un même plan les atomes participant à la cyclisation, soit : le C1, le C5 et l'Oxygène du C5.</td>
</tr>
</table></td></tr></table>
Le cycle à 6 sommets qui en résulte est appelé pyranique car il est issu du pyrane.1.4.7 Intérêt de la structure cyclique
La structure cyclique explique les objections à la structure linéaire des oses et les propriétés de ceux-ci :
- La
fonction aldéhyde ou cétonique de l'ose, partiellement dissimulée
(hémiacétal), est appelée pseudoaldéhydique ou pseudocétonique.
- Il existe un carbone asymétrique (C1 des aldoses ; C2 des cétoses) en raison de l'hémiacétalisation interne qui conduit à 2 anomères :
 et ß et ß
- L'anomère

a un OH hémiacétalique du même côté que le OH porté par le C
subterminal qui détermine la série. Il a le pouvoir rotatoire le plus
élevé.
L'anomère ß a les propriétés inverses.
1.4.8 Structure cyclique des oses selon Haworth:
Deux structures cycliques sont possibles.
- La forme pyranique correspond à un hérérocycle à 6 sommets (5 C et 1 O).
- La forme furanique correspond à un hétérocycle à 5 sommets (4 C et 1 O).
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
1.4.8.1 D Glucopyranose:
- Le Glucose naturel (D (+) Glucose) est très
répandu dans la nature. C'est le principal carburant de l'organisme et
le carburant universel du foetus.
- La polymérisation du Glucose conduit au Glycogène (foie, muscles).
- La glycémie est la concentration de Glucose à l'état libre dans le sang (0,80g/L soit 4,4 mM/L).
- Le Glucose est réducteur. La Glucose oxydase l'oxyde en acide aldonique :
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
- Son pouvoir rotatoire est dextrogyre.
1.4.8.2 D-Galactopyranose:
- Il intervient dans la composition de :
- Lactose = D Gal + D Glc
- Cérébrogalactosides du cerveau
- Certains glycolipides et glycoprotéines
</li>
Son pouvoir rotatoire est dextrogyre.
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
1.4.8.3 D-Mannopyranose:
- Il est présent surtout dans les végétaux.
- C'est un constituant des glycoprotéines chez l'homme.
- Son pouvoir rotatoire est dextrogyre.
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
1.4.8.4 D-Fructofuranose:
- On le trouve surtout dans les fruits d'où son nom.
- Son pouvoir rotatoire est lévogyre d'où son nom de Lévulose.
- Il est présent dans le liquide spermatique chez l'homme où il participe au mouvement des spermatozoïdes.
- Il est présent sous forme furanique dans le saccharose.
- La cyclisation se fait entre le C2 (cétone) et le C5.
<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
1.4.8.5 D Ribofuranose:
- La forme furanique est la forme habituelle des pentoses combinés dans les acides nucléiques (ARN).
- Le ßD Ribofuranose est lié aux bases puriques et pyrimidiques par une liaison N-osidique (nucléosides, nucléotides).
- Il intervient dans la structure des coenzymes : NAD, NADP, ATP.
La forme biologique est la forme furanique (1 - 4):<table align="center" border="0" cellpadding="0" cellspacing="2">
<tr align="center"><td> </td> </td>
</tr></table>
- Dans le Désoxyribose le OH en 2 est remplacé par H (ADN).
  
</td>
</tr></table>
|

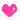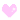
 Aldose ; Cétone
Aldose ; Cétone  Cétose
Cétose

 </td>
</td> 2 tétroses
2 tétroses  4 pentoses
4 pentoses  8 hexoses).1.4.4 Principaux oses naturels selon Fischer:
8 hexoses).1.4.4 Principaux oses naturels selon Fischer: </td>
</td>
 </td>
</td> </td>
</td> </td>
</td> </td>
</td> </td>
</td> </td>
</td>





 </td>
</td> </td>
</td> </td>
</td> </td>
</td> ou ß à l'origine de la mutarotation. Ces 2 anomères différent par la position dans l'espace du OH hémiacétalique.
ou ß à l'origine de la mutarotation. Ces 2 anomères différent par la position dans l'espace du OH hémiacétalique. </td>
</td> </td>
</td>